produit de solubilité ks
|
SMPC (S2) Année universitaire : 2019/2020 Cours de chimie des
Le produit de solubilité Ks est la constante d'équilibre de la réaction écrite dans le sens de la dissolution du solide ionique dans l'eau. Exemple :. |
|
Précipitation et produit de solubilité
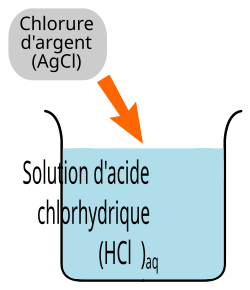
Précipitation et produit de solubilité. I - Produit de solubilité. Dans une solution saturée de chlorure d'argent AgCl solide coexiste avec AgCl dissous |
|
Equilibre : Précipitation-Solubilité /Dr. Maghchiche
Tableau 1 : produit de solubilité de quelques sels. Sel. Ks. Sel. Ks. AgCl. AgBr. AgI. AgSCN. Ag2CrO4. CaSO4. |
|
Produit de solubilité de la calcite et constantes de dissociation de
- fixation d'un ensemble de valeurs arbitraires de Ks K3 et K4 |
|
Diapositive 1
Le produit des concentrations [Cn+]m [Am-]n est inférieur à Ks. Exemple: La solubilité du chromate d'argent Ag2CrO4 dans l'eau à 25 ° est 0 |
|
Chapitre 1 Solubilité
Cette équilibre est appelé équilibre de solubilisation il est caractérisé par une constante d'équilibre Ks(T) appelé produit de solubilité et s'exprimant |
|
CHIM105B – DS2 – Corrigé
- l'ion hydroxyde OH- |
|
Précipitation et solubilité
on peut écrire le produit de solubilité. De plus la concentration en cation y vaut encore c = 0 |
|
CaCO + C + ( ) =
Remarque : dans l'équilibre ci-dessus la réaction de l 'eau avec les ions fluorure a été négligée. 2.2) Produit de solubilité Ks. Soit une solution saturée en |
|
Biologie cellulaire. Exercices et méthodes
Le produit de solubilité du phosphate de zinc s'exprime par la relation Dès lors le produit de solubilité du carbonate d'argent Ks (Ag2CO3) = [Ag+]. |
|
CHAPITRE II Equilibres de solubilité et de complexation I
Dans ce cas la solubilité dépend de la concentration en ions OH-et donc du pH [OH-]= (Ks / [Mg2+])1/2 Exercice 4 Mg(OH) 2(S) a un produit de solubilité Ks = 1 8 10-11 1- On ajoute une base à une solution contenant 05 mol/L de chlorure de magnésium MgCl 2 (Sel totalement soluble dans l’eau) à quele valeur de pH commencera la |
|
Chapitre Chapitre II: II: La La solubilité solubilité
2 Aspect quantitatif de la solubilité: 2 2 Définition de la solubilité: La solubilité S d’un cristal ionique (un sel peu soluble) dans l’eau est le nombre de moles du composé ionique capable de se dissoudre dans un litre de solution exprimé en mol L-1 3 2 produit de solubilité Ks Certains composés ioniques mis en solution aqueuse |
|
LC 27 – Solubilité
2 1 Le produit de solubilité Dé?nition : produit de solubilité Le produit de solubilité Kscorrespond à la constante d’équilibre de dissolu-tion du précipité en ses deux ions Application : chlorure d’argent On écrit l’équation de solubilisation : AgCl (s) = Ag(aq) + +Cl?(aq) Le produit de solubilité de AgCl s’écrit : K s |
|
Solubilité & produit de solubilité
1 Solubilité et produit de solubilité Certains Sels ou hydroxydes sont peu solubles dans l'eau : AgC1 ; PbC12 BaS04 ; ; ; Ag(OH) On parle alors d'un équilibre de dissolution Oil deux phases coexistent qui contient les ions solvatés dissous et la phase solide : la phase aqueuse Solubilité s (en mol L—l) : nombre maximal de moles |
|
Searches related to produit de solubilité ks PDF
Le produit de solubilité Ks est la constante d’équilibre de la réaction écrite dans le sens de la dissolution du solide ionique dans l’eau Exemple : Pour un solide pur l’activité est toujours égale à 1 Ks = f(T) On pose : pKs = - log Ks Ks = 10-pKs Plus Ks est petit plus le pk s est grand moins le sel est soluble |
Qu'est-ce que le produit de solubilité?
Le produit de solubilité Ks est la constante d’équilibre de la réaction écrite dans le sens de la dissolution du solide ionique dans l’eau. Exemple : Pour un solide pur, l’activité est toujours égale à 1.
Quelle est la relation entre le K S et la solubilité ?
La relation générale entre le K s et la solubilité est la suivante : . Quel est le comportement d'un composé que l'on dissout dans une solution qui contient préalablement un ion de ce composé ?
Quelle est la valeur du produit de solubilité ?
La valeur du produit de solubilité dépend de la température. De façon générale, elle croît avec la température. Le produit de solubilité est un rapport de concentrations. C'est donc un nombre sans dimension, qui s'exprime sans unité. Il s'agit d'une constante thermodynamique intervenant dans la loi d'action de masse .
Comment calculer la constante du produit de solubilité ?
La constante de cet équilibre est appelée constante du produit de solubilité, Kps. Le terme «produit» désigne la multiplication des concentrations des ions qui composent le solide: Kps= [Pb2+] [JE–]2 Ici, le solide est constitué des ions exprimés dans l'équation; cependant, il ne tient pas compte du solide dans ces calculs.
| SOLUBILITE / PRECIPITATION |
| SOLUBILITE / PRECIPITATION - ?????? ????? ??????? |
| CHAPITRE II Equilibres de solubilité et de complexation I |
| SOLUBILITY PRODUCT CONSTANTS - Université Laval |
| Précipitation - Produit de solubilité A – Introduction |
Comment calculer la solubilité du dioxyde de carbone?
- Remarque importante: les constantes d’équilibre et la solubilité du dioxyde de carbone dépendent toutes de la température Dans le domaine de prédominance des ions carbonate : (la solubilité est notée s3) [Ca ] s2 Ks[]termes négligeables1 3 2+2 = =+ d’où l’on tire : 2 ps pKs
|
II- Solubilité et produit de solubilité 1- Définition
Le produit de solubilité (ou la constante de solubilité) noté « Ks » d'un solide ionique correspond à la constante d'équilibre de la réaction de dissolution de ce |
|
Précipitation - Produit de solubilité A – Introduction - Nicole Cortial
Le produit de solubilité s K du solide )( snq XM correspond à la constante d' équilibre de la réaction de dissolution de ce solide : − + ← → + q n snq Xn Mq |
|
Ks - univ-biskra
Calculer le produit de solubilité du chromate d'argent Ag=108; Cr=52; O=16 gmol -1 Ag2CrO4 solide en équilibre avec 2Ag+ + CrO4 2- masse molaire Ag2CrO4 : |
|
SOLUBILITE / PRECIPITATION
Tableau 1 : Produit de solubilité de quelques composés peu solubles Sel Expression de k SP Valeur de K Sp pK Sp AgCl K SP = [Ag+] [Cl-] 1,8 10-10 |
|
Précipitation et produit de solubilité
Précipitation et solubilité 1/5 Précipitation et produit de solubilité I - Produit de solubilité Dans une solution saturée de chlorure d'argent, AgCl solide coexiste |
|
Semestre 2 – Chapitre 4 : Équilibres de solubilité La notion intuitive
1- Lorsqu'on dissout dans l'eau de l'hydroxyde de magnésium (II) Mg(OH)2 (s) jusqu'à saturation, la solution possède un pH égal à 10,5 Montrer que le produit de |
|
Produit de solubilité de la calcite et constantes de - Érudit
Les valeurs du produit de solubilité de la calcite et des constantes de dissociation de CaHCO3+ et CaCO30, notées K3 et K4, ont été déterminées à différentes |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
On appelle produit de solubilité, noté Ks, la constante d'équilibre associée à l' équilibre entre le solide –le précipité-‐ et ses ions en solution aqueuse : Equilibre |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
détermination du produit de solubilité de l'iodate de lanthane à 298 K A 25°C, la concentration des ions La3+ d'une solution saturée d'iodate de lanthane |








![PDF] Produit de solubilité de la calcite et constantes de PDF] Produit de solubilité de la calcite et constantes de](https://d3i71xaburhd42.cloudfront.net/60711001bf6d962e1fa476a2e77871d2cc90c892/11-Figure3-1.png)





![PDF] Produit de solubilité de la calcite et constantes de PDF] Produit de solubilité de la calcite et constantes de](https://d3i71xaburhd42.cloudfront.net/60711001bf6d962e1fa476a2e77871d2cc90c892/12-Table3-1.png)


![PDF] Produit de solubilité de la calcite et constantes de PDF] Produit de solubilité de la calcite et constantes de](https://d3i71xaburhd42.cloudfront.net/60711001bf6d962e1fa476a2e77871d2cc90c892/10-Figure2-1.png)


