liste acide fort acide faible pdf
Comment classer les acides forts ?
Acide fort et base forte
Un acide ou une base est qualifié(e) de fort(e) si sa réaction avec l'eau est totale. À l'état final de cette transformation, l'acide nitrique est absent car il a été complètement consommé.
Sa réaction avec l'eau a donc été totale, ce qui justifie sa nature d'acide fort.Quels sont les acides fort et faible ?
Un acide appartenant à un couple acide-base de négatif sera donc totalement transformé en ions H 3 O + : on dit qu'il s'agit alors d'un acide fort.
Un acide appartenant à un couple acide-base de positif ne sera que partiellement transformé en ions H 3 O + : on dit qu'il s'agit alors d'un acide faible.
|
Les acides et bases en solution aqueuse.
d'identifier dans une liste donnée |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
Acides forts et bases fortes
Un acide libère des protons H+ pour former des ions oxonium ( ou hydronium) H3O+ Les acides faibles ne se dissocient pas totalement dans l'eau. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'un acide fort. 2.2. Cas d'un acide faible. 2.3. Cas d'une base forte. 2.4. |
|
Transformations chimiques en solution aqueuse
II – LA REACTION ACIDE/BASE. 8. 1. LES ACIDES FORTS ET LES BASES FORTES. 8. 2. LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE D'ACIDITE ASSOCIEE. |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
ANNALES SCIENCES PHYSIQUES Terminale D
Chapitre 6 : L'étude de la réaction entre un acide faible et une base forte une base faible et un acide fort. CHIMIE ORGANIQUE. Chapitre 7 : Les alcools. |
|
Acide phosphorique
L'acide phosphorique est un triacide minéral. La première fonction est celle d'un acide fort la deuxième celle d'un acide faible et la troisième celle d'un |
|
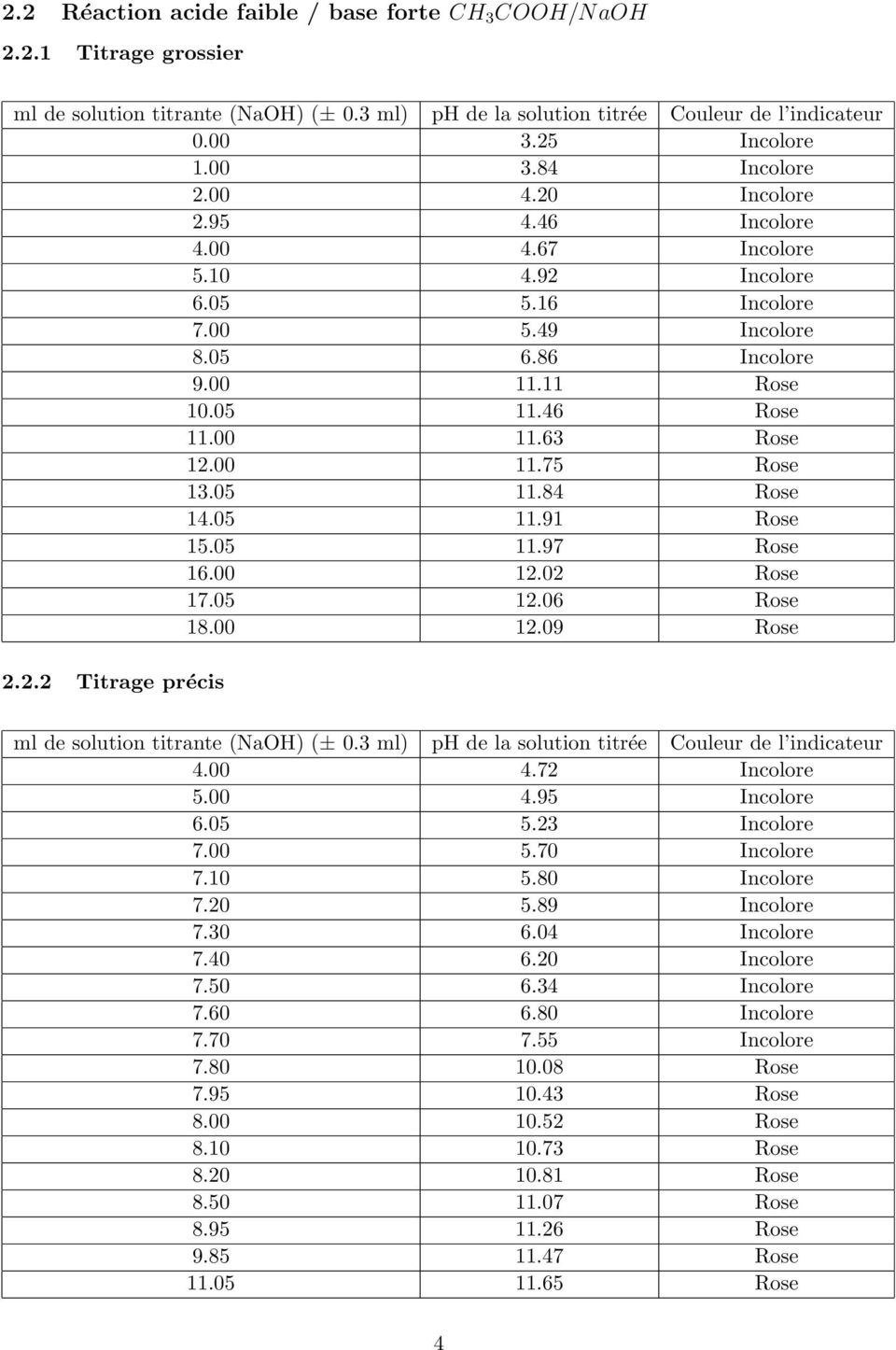
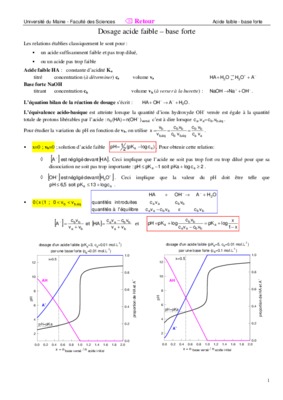
Cours de Chimie - Informatique Titrage acide/base
17 avr. 2013 Dans le cas du titrage d'un acide fort par une base forte ... Le pH d'une solution d'acide faible comme CH3COOH se calcule d'après la. |
|
Les acides et bases en solution aqueuse - Groupe Transition
distribuer gratuitement un ou plusieurs fichiers PDF ou ZIP complets et sans modification d'identifier, dans une liste donnée, les acides et les bases selon Coefficient d'ionisation (de dissociation) d'un acide ou d'une base faible Comme NaOH et HCl sont des électrolytes forts, l'équation ionique doit s'écrire : Na + |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Propriétés des acides et des bases
•pKa = -log (Ka) ou Ka =10 (- pKa) montre que pKa et Ka varient en sens contraires : •pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide faible |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Les acides et les bases - La chimie
Les acides forts et les bases fortes • un acide fort est un électrolyte fort qui s' ionise complètement dans l'eau • ex ; HCl, HNO 3 , H 2 SO 4 • un acide faible |
|
Acides forts et bases fortes
La réaction n'est donc pas totale Les acides faibles sont d'autant moins dissociés dans l'eau qu'ils sont concentrés L'effet de la dilution tend |
|
VIEtude sommaire des mélanges
2) Acide fort 1 + acide faible 2 On calcule souvent le pH en négligeant l'acide faible Cette approximation grossière n'est justifiée que si l'apport d'ions |
|
R E A C T I O N S A C I D O – B A S I Q U E S
Une base forte dans l'eau va entièrement se dissocier et une base faible va se ioniser de façon partielle dans l'eau (cf figure ci-dessous) 1-3 Couples acide- base |