obtenir de l'eau pure 5eme
|
ACTIVITE N°6 une eau limpide est-elle une eau pure
La distillation permet de séparer les constituants d'un mélange homogène Grace à cette méthode on peut obtenir une eau pure à partir d'une eau minérale |
|
C5-ETUDE DES CHANGEMENTS DETAT_Exercices-Livre
La température de solidification de l'eau pure est 100 °C / 0 °C Elle varie / est constante au cours du changement d'état 5 Remettre un peu d'ordre |
|
Chapitre 1 : Leau que nous buvons est-elle pure ?
29 nov 2020 · L'eau pure et les eaux que l'on peut boire L'eau que nous buvons n'est pas un corps pur mais un mélange d'eau et de sels minéraux dissouts L |
|
Chapitre 2 : Comment obtenir de leau pure ?
On met un peu de sirop de menthe (vert) dans un tube a essai contenant de l'eau On bouche le tube et on agite vigoureusement On laisse ensuite reposer |
|
Chapitre Chimie 52 : Leau
Chapitre Chimie 5 2 : L'eau 1 Quels sont les états physiques de la matière ? 2 Sous quel état est l'eau des nuages ? 3 A quoi ressemble la vapeur d'eau |
|
CHP 3 : mélanges homogènes et corps purs mélanges homogènes
Si l'on souhaite obtenir de l'eau pure il faut procéder à une distillation Le principe est simple : il consiste à récupérer la vapeur d'eau qui s'échappe lors |
|
CYCLE 4
Doc 1 - Issue d'un site unique au cœur des Alpes Evian est une eau minérale naturellement pure Elle ne subit aucun traitement et n'est jamais touchée par |
|
Les-changements-détatpdf
Pour l'eau pure les températures de changement d'état sont sous la pression atmosphérique normale (1 013 hPa) : - solidification et fusion : 0 °C ; - |
Comment obtenir de l'eau pure ?
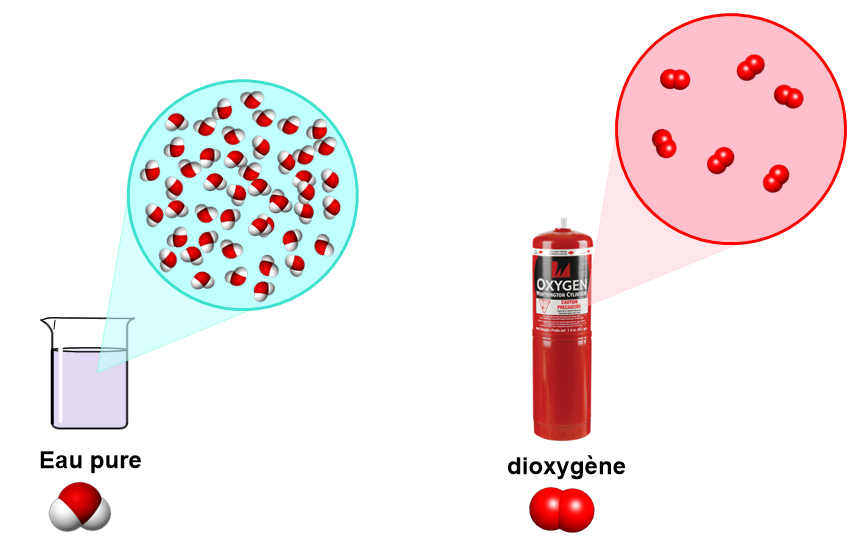
Une eau pure est de l'eau douce ne contenant que la molécule H2O et aucun autre élément chimique.
Elle est exempte de toute autre substance chimique tels que des matières dissoutes (impuretés), sels, minéraux Son obtention se fait par ébullition, distillation, désionisation et osmose inverse.Comment est constitué l'eau pure ?
En physique, le terme « eau pure » désigne une eau dont la molécule H²0 est le seul composant.
C'est une eau non altérée, non polluée et qui n'est entrée en contact avec aucune autre substance, quelle qu'elle soit.Comment obtenir une eau pure à partir d'une eau limpide ?
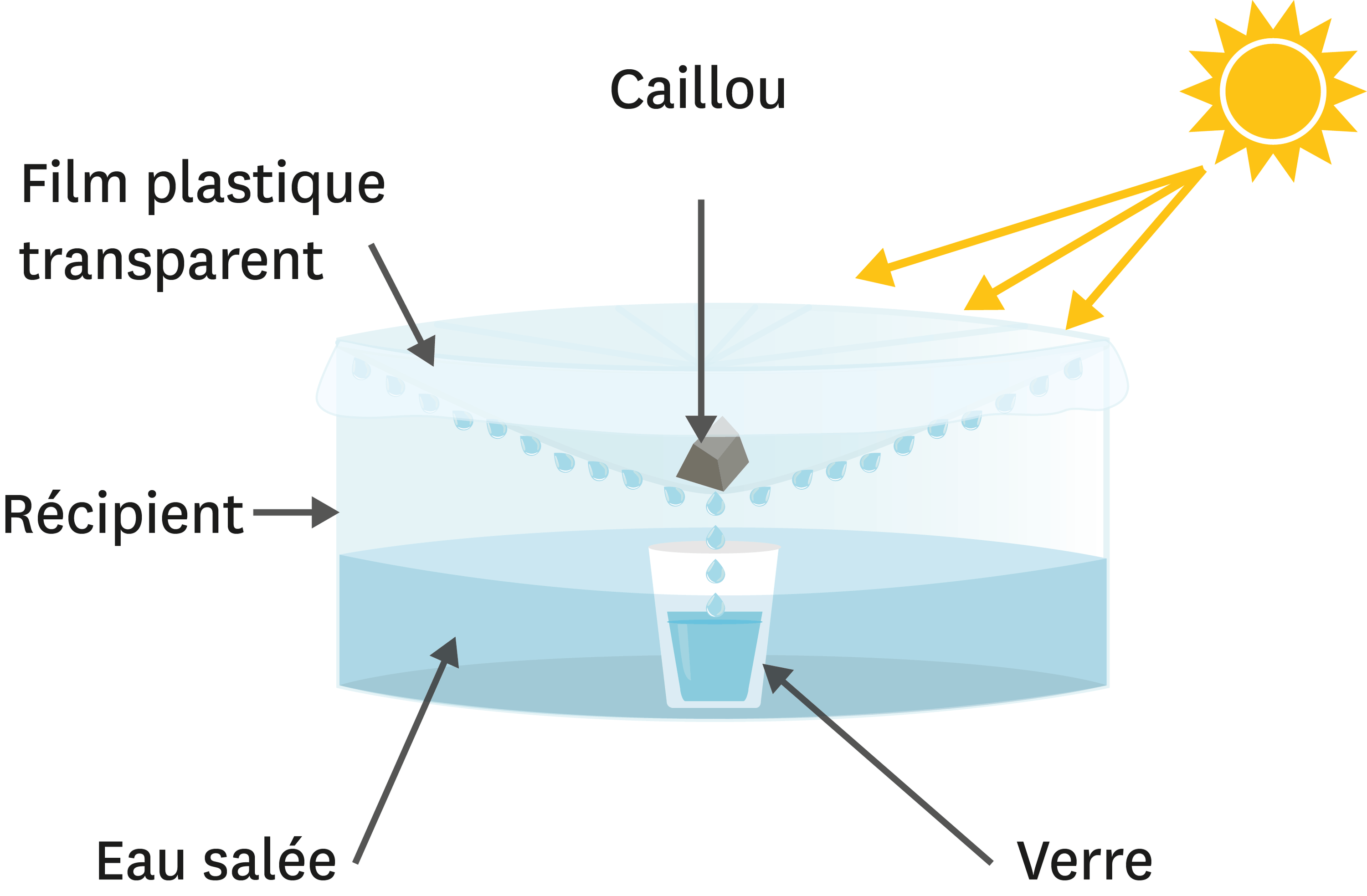
Principe d'une distillation :
L'eau liquide du mélange homogène se transforme en vapeur d'eau.
La vapeur d'eau passe ensuite dans le réfrigérant, ou elle se refroidit.
Elle se condense, et on s'écoule dans le bécher : c'est de l'eau pure.
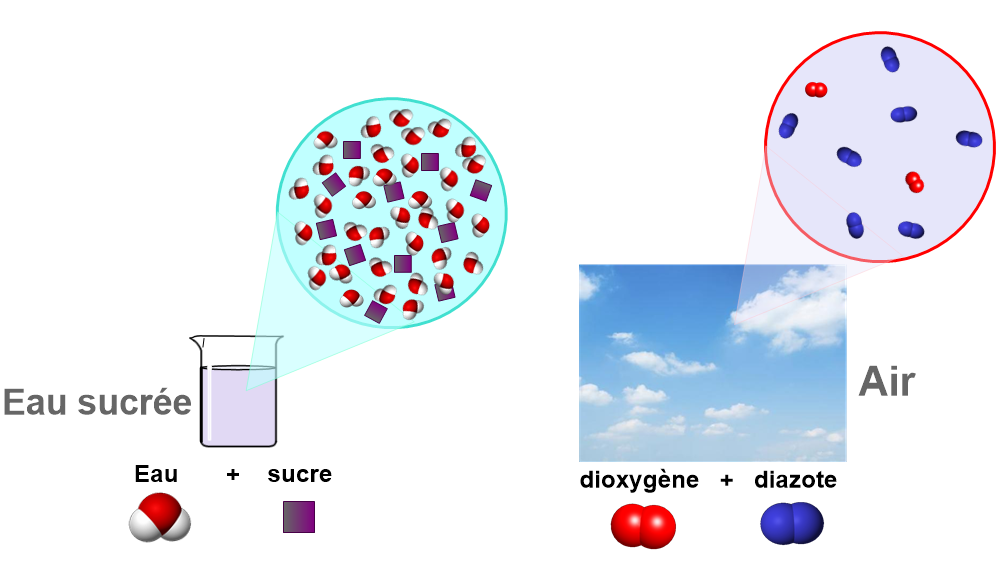
Le liquide limpide obtenu est appelé distillat, et est constitué d'eau pure.- Un corps pur est une substance composée d'un seul type d'espèce chimique (atomes ou molécules).
L'eau déminéralisée (ou distillée) est un corps pur, car elle n'est composée que de molécules d'eau.
|
CHP 3 : mélanges homogènes et corps purs mélanges homogènes
Si l'on souhaite obtenir de l'eau pure il faut procéder à une distillation. Le principe est simple : il consiste à récupérer la vapeur d'eau qui s'échappe lors |
|
ACTIVITE N°6 une eau limpide est-elle une eau pure
Comment obtenir de l'eau pure à partir d'une eau minérale ? 1. Mise en œuvre expérimentale : la distillation. On place un mélange homogène ou hétérogène (eau |
|
CYCLE 4 - Classe de 5ème Activités de chimie mélanges/corps pur
Après avoir remué : On ne voit qu'un seul liquide (*) … 4- Conclus (explique que les liquides sont miscibles) : Quand on remue (*) le cocktail on s' |
|
Chapitre 1 : Leau que nous buvons est-elle pure ?
29 nov. 2020 L'EAU PURE ET LES EAUX QUE L'ON PEUT BOIRE. ... Aulnay-Sous-Bois – Cinquième – Physique-chimie. 1. Chapitre 1. : L. 'eau q ue nous b. |
|
Chap 10 - Comment obtenir de leau pure à partir dune eau boueuse
Pour obtenir de l'eau pure nous allons le distiller. Activité : distillation d'une eau boueuse. •. Qu'arrive-t-il au liquide |
|
Chapitre 2 : Comment obtenir de leau pure ?
L'eau et le sirop de menthe sont des liquides miscibles entre eux ils ne forment qu'une seule phase lorsqu'on les mélange. Conclusion : Un mélange homogène est |
|
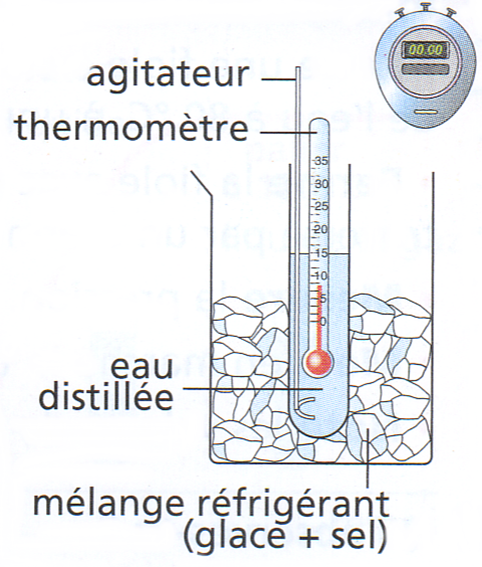
SOLIDIFICATION et FUSION 1. Solidification de leau pure
1. Solidification de l'eau pure. Expérience : On place un tube à essai contenant de l'eau dans un mélange réfrigérant {glace + sel}. |
|
SEPARATION DES CONSTITUANTS DUN MÉLANGE HOMOGÈNE
5ème. SEPARATION DES CONSTITUANTS D'UN MÉLANGE HOMOGÈNE Toutes les eaux minérales contiennent des substances solides ... OBTENIR DE L'EAU PURE. |
|
Physique Chimie
8 fév. 2017 pour obtenir un sirop ayant le même goût sucré ? Une solution. 1 Le soluté est le sucre. 2 Le solvant est l'eau. |
|
Chapitre C2 – LES MELANGES AQUEUX Aqueux : à base deau
COMMENT OBTENIR DE L'EAU PURE A PARTIR D'UN MELANGE HETEROGENE ? Exercice 6 page 125 (Nathan Physique Chimie 5ème |
|
Chapitre 1 : Leau que nous buvons est-elle pure ?
29 nov 2020 · Pour détecter la présence d'eau dans un aliment solide ou liquide on met en contact du sulfate de cuivre anhydre (une poudre blanche) avec l' |
|
ACTIVITE N°6 une eau limpide est-elle une eau pure - gouet-physique
Comment obtenir de l'eau pure à partir d'une eau minérale ? 1 Mise en œuvre expérimentale : la distillation On place un mélange homogène ou hétérogène (eau |
|
Chapitre II - Les changements détat de leau
La fusion et la solidification de l'eau pure se produisent à la même température : 0°C V – Étude de l'ébullition de l'eau pure Si on chauffe un liquide on |
|
En classe de 5ème - Leau dans notre environnement
Comprendre ce qu'est un corps pur – Connaître et comprendre les changements d'états de l'eau – Savoir dissoudre un solide dans l'eau et mélanger l'eau |
|
Chapitre Chimie 52 : Leau
Chapitre Chimie 5 2 : L'eau 1 Quels sont les états physiques de la matière ? 2 Sous quel état est l'eau des nuages ? 3 A quoi ressemble la vapeur d'eau |
|
CHP 3 : mélanges homogènes et corps purs mélanges homogènes
Si l'on souhaite obtenir de l'eau pure il faut procéder à une distillation Le principe est simple : il consiste à récupérer la vapeur d'eau qui s'échappe lors |
|
C5-ETUDE DES CHANGEMENTS DETAT_Exercices-Livre
corps pur / mélange 2 La température de solidification de l'eau pure est 100 °C / 0 °C Elle varie / est constante au cours du changement d'état |
|
SOLIDIFICATION et FUSION - PCCL
Solidification de l'eau pure Expérience : On place un tube à essai contenant de l'eau dans un mélange réfrigérant {glace + sel} |
|
CYCLE 4 - Classe de 5ème Activités de chimie mélanges/corps pur
CETTE EAU QUALIFIEE DE PURE PAR LES PUBLICITAIRES N'EST PAS CONSIDEREE COMME PURE PAR LES CHIMISTES MAIS COMME UN MELANGE |
|
5ch12cpdf
n lors de la fusion de la glace ? Lq cswbe ? idification de l'eau pure ? température (en' |
Comment Obtient-on une eau pure ?
Comment savoir si un liquide est constitué d'eau pure ? (5eme) Il faut faire appel aux caractéristiques de l'eau. On peut vérifier que la masse du liquide correspond à 1 kg pour un litre. Si l'ébullition du liquide se fait à une température constante de 100 °C, alors il s'agit d'eau pure.Comment savoir si l'eau est pure 5eme ?
Il est possible pour les particuliers de se procurer de l'eau pure dans le commerce. Certaines entreprises proposent en effet de l'eau purifiée à l'achat. Toutefois, la méthode la plus courante pour obtenir de l'eau purifiée est simplement de le faire soi-même en utilisant les techniques disponibles.Où se procurer de l'eau pure ?
En physique, le terme « eau pure » désigne une eau dont la molécule H? est le seul composant. C'est une eau non altérée, non polluée et qui n'est entrée en contact avec aucune autre substance, quelle qu'elle soit.
Comment savoir si l'eau est pure 5eme ?
. On peut vérifier que la masse du liquide correspond à 1 kg pour un litre. Si l'ébullition du liquide se fait à une température constante de 100 °C, alors il s'agit d'eau pure.
Quand l'eau est pure ?
. C'est une eau non altérée, non polluée et qui n'est entrée en contact avec aucune autre substance, quelle qu'elle soit.
Comment se décompose l'eau pure ?
. La quantité de dihydrogène gazeux produite est donc équivalente à deux fois la quantité de dioxygène.
Quels sont les 4 changement d'état de l'eau ?
. La fusion est le passage de l'état solide à l'état liquide.
. La vaporisation est le passage de l'état liquide à l'état de vapeur.
. La liquéfaction est le passage de l'état de vapeur à l'état liquide.
|
Chapitre 2 Obtenir de leau pure
AE Comment obtenir de l'eau limpide (qui n'est pas trouble) à partir d'une eau boueuse ? Proposer par écrit une ou plusieurs expériences Activité 2p23 Comment |
|
Chapitre 2 Obtenir de leau pure
Chapitre 2 Obtenir de l'eau pure Item Connaissances Acquis Mélanges homogènes et hétérogènes Décantation Filtration Une eau d'apparence homogène |
|
Chap 10 - Comment obtenir de leau pure à partir dune eau boueuse
A court d'eau potable, ils cherchent une source mais ne trouvent que des marres d'eau boueuse Assis au bord de l'eau, ils se demandent que faire L'heure est |
|
Chapitre 2 : Comment obtenir de leau pure ? - MMorin
Chapitre 2 : Comment obtenir de l'eau pure ? I) Comment distinguer un mélange homogène d'un mélange hétérogène : Définition : Un mélange aqueux est une |
|
CHP 3 : mélanges homogènes et corps purs mélanges homogènes
5ème CHP 3 : mélanges homogènes et corps purs mélanges homogènes et corps purs mélanges II) Comment récupérer de l'eau pure à partir d'une eau minérale ? Si l'on souhaite obtenir de l'eau pure il faut procéder à une distillation |
|
Classe de 5ème Activités de chimie mélanges/corps pur Explicatifs
1 - Issue d'un site unique au cœur des Alpes, Evian est une eau minérale naturellement pure Elle ne subit aucun traitement et n'est jamais touchée par la main de |
|
Exercices Ch3 LES MELANGES HOMOGENES - Physique-Chimie
Obtenir de l'eau pure (voir paragraphe 2 du cours) p : 40 n°5 Réaliser une distillation avec de l'eau minérale 1 Lors de la distillation d'une eau minérale, |
|
Chapitre 1: Matière, corps purs et mélanges
Un corps pur peut être identifié grâce à ses propriétés (voir chapitre 4) Voici quelques exemples de corps purs : le fer, l'eau distillée et le chlorure de sodium ( sel de La distillation est un procédé qui permet d'obtenir des liquides purs à partir |
|
10 LA PURETÉ DE LEAU
Goûter l'eau pour savoir s'il y a des impuretés HYPOTHÈSE Je prédis que l'eau pure n'aura pas de goût et je goûterai le sel ou le sucre |
|
Comment rendre limpide une eau boueuse
Niveau : cinquième Partie A, MELANGES AQUEUX : Comment obtenir de l'eau limpide ? Dans l'étape suivante on obtiendra de l'eau pure par distillation |