tp loi de beer lambert 1ere s
|
1 La spectrophotométriepdf
3 4-1- loi de Beer-Lambert La loi de Beer-Lambert est une relation empirique reliant l'absorption de la lumière aux propriétés des milieux qu'elle traverse |
|
Activité expérimentale
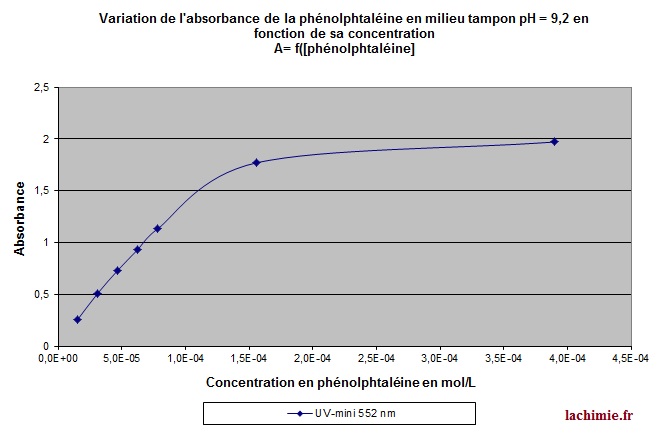
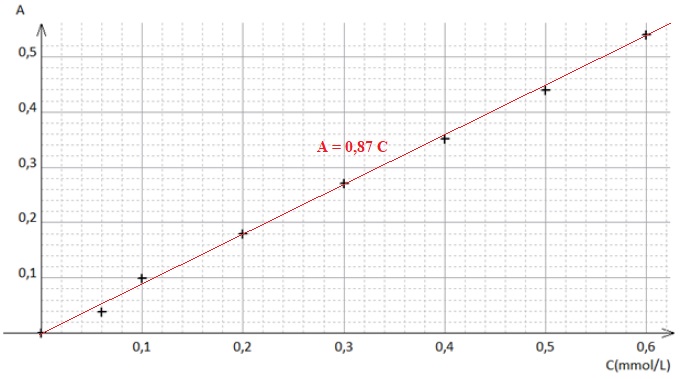
Nous pouvons donc constater que la loi de Beer- Lambert est limitée aux faibles concentrations y = 80482x 0 005 01 015 0 |
|
TP C1 : Spectrophotométrie Loi de Beer-Lambert
22 sept 2005 · Le but de ce TP est de (re)découvrir expérimentalement la loi de Beer- Lambert qui établit une relation entre absorption longueur du trajet |
|
TP Comment déterminer la concentration dun principe actif
Doc 3: Spectrophotométrie: loi de Beer-Lambert L'absorbance A d'une solution colorée est proportionnelle à la concentration molaire C de l'espèce chimique |
|
TP en Première S (option sciences expérimentales) Vérification de
Aussi après réflexion a-t-il été possible de réaliser au lycée avec «les moyens du bord» une manipulation visant à vérifier la loi de Beer-Lambert Cette |
|
TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
On obtient alors une loi appelée loi de Beer-Lambert : A = ε×l×c Le coefficient directeur de la droite correspond au produit ε×l 8) Est-ce que la courbe |
Comment mesurer l'absorbance TP ?
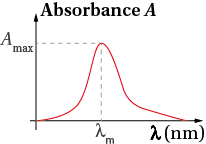
On utilise comme matériel un spectrophotomètre.
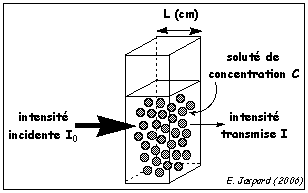
Le spectrophotomètre sélectionne une radiation monochromatique (une seule longueur d'onde λ) à travers une cuve de longueur l de solution et mesure l'absorbance A de la solution.
Il faut régler le zéro en plaçant le solvant (eau) dans la cuve.Comment calculer avec la loi de Beer-Lambert ?
Parfois, la loi de Beer-Lambert est écrite sous la forme A = k \\times C dans laquelle la constante k est le produit du coefficient d'extinction molaire \\varepsilon et de la longueur l de solution traversée : k = \\varepsilon \\times l.
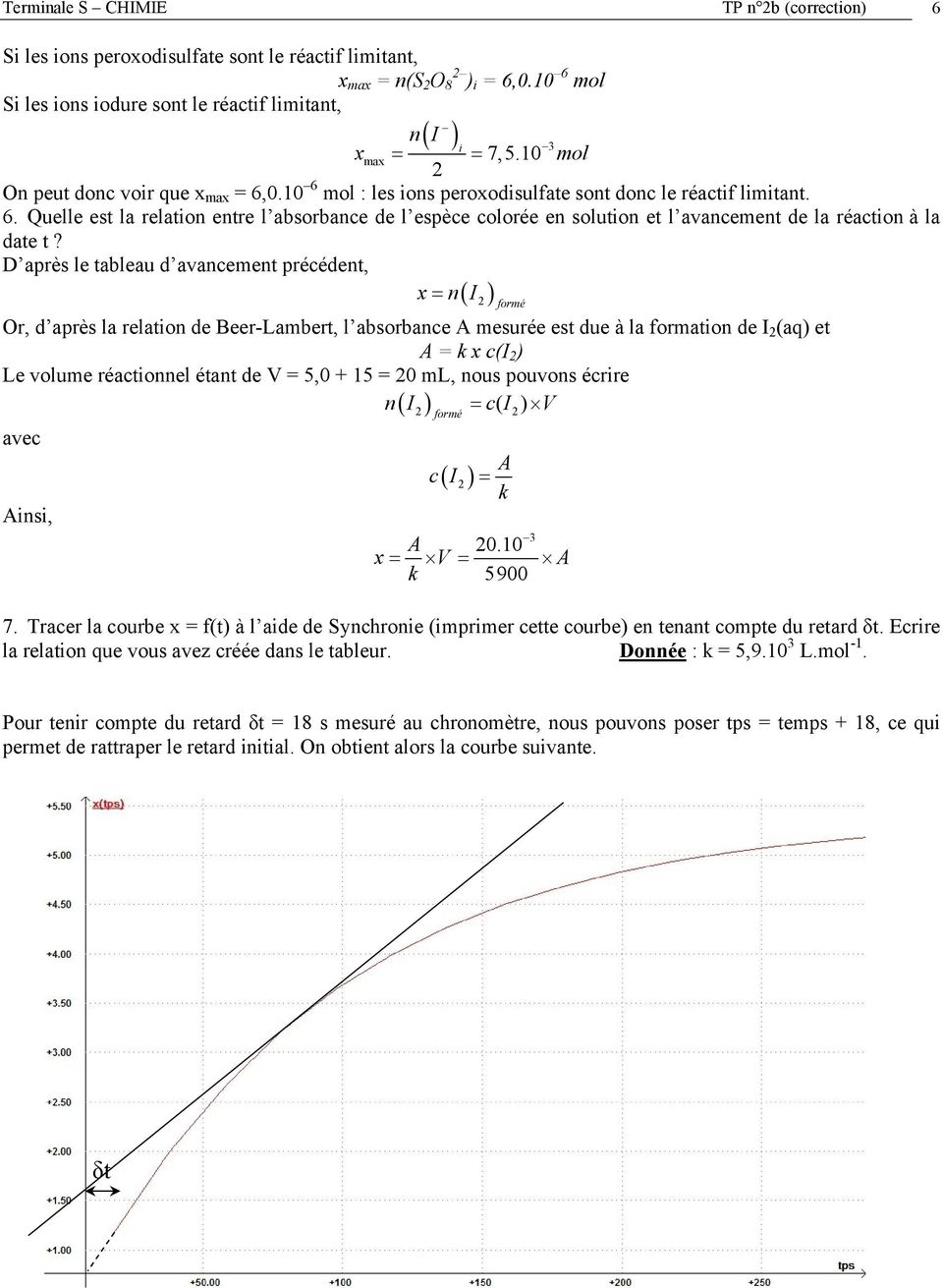
- Par conséquent cette méthode peut être utilisée lorsqu'une espèce colorée se forme ou disparaît au cours de la réaction comme la réaction entre l'eau oxygénée et les ions iodure : il se forme du diiode qui est une espèce chimique colorée.
|
TP C1 : Spectrophotométrie Loi de Beer-Lambert
22 sept. 2005 10−4 mol/L. Fig. 3 – Schéma du dispositif expérimental de mesure de l'inluence de la lon- gueur du trajet optique sur l'absorbance. |
|
T.P. en Première S (option sciences expérimentales) Vérification de
Aussi après réflexion |
|
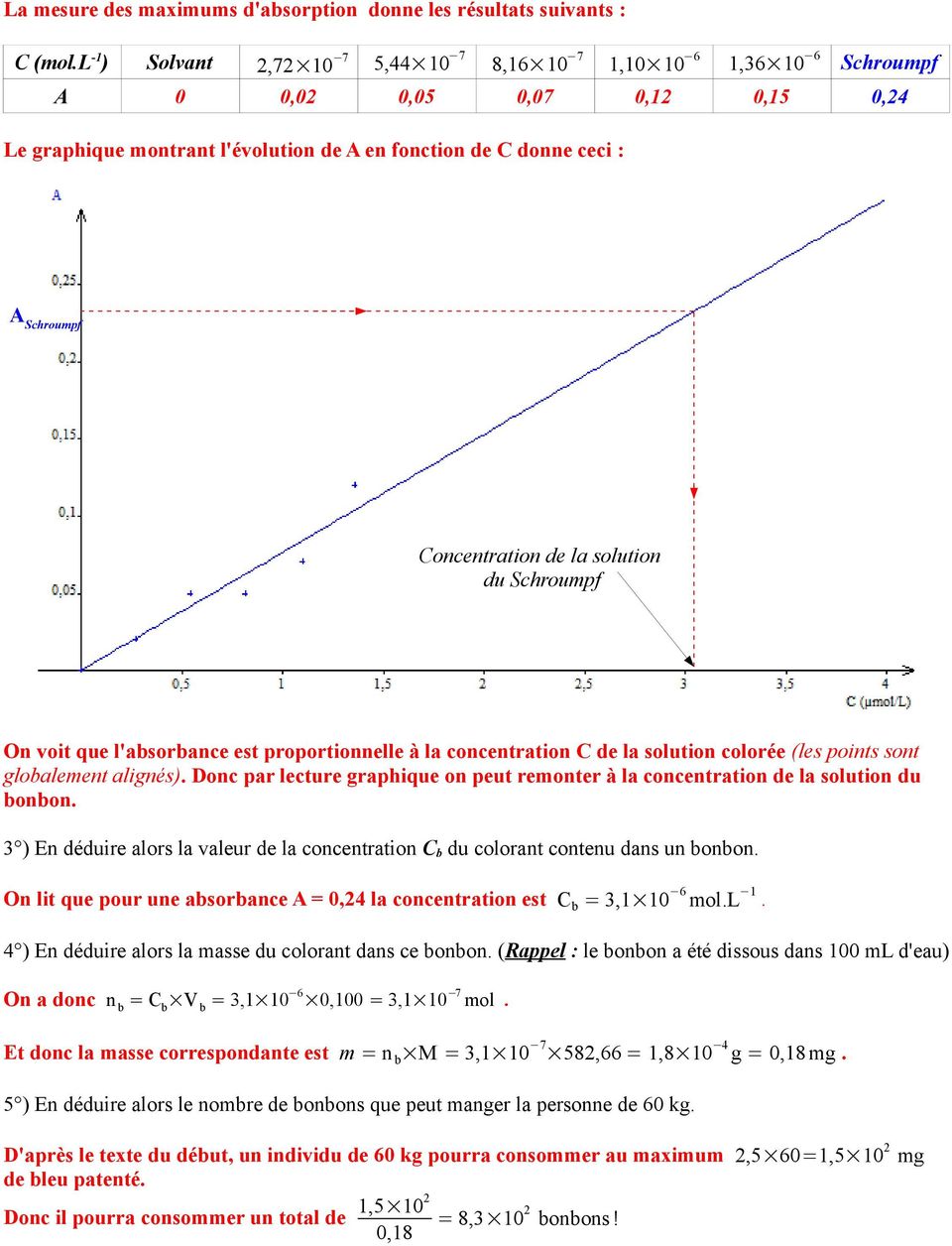
Le bleu des bonbons Schtroumpfs
Cette séance de réinvestissement intervient après l'étude expérimentale de la loi de Beer-Lambert. En revanche si les résidus semblent suivre une loi et ne s' ... |
|
Loi de Beer-Lambert
Enfin l'analyse de. Page 21. Lycée voie(s). Générale. Technologique Professionnelle. CAP. Seconde. Première. Terminale. Physique-chimie eduscol.education.fr. |
|
Dosage par étalonnage loi de Beer-Lambert
Dosage par étalonnage. Loi de Beer-Lambert. Objectifs du T.P. : Savoir calculer une masse à dissoudre pour obtenir une solution de concentration donnée. |
|
OBSERVER : Notions compétences et activités (première S).
21 nov. 2016 utilisant la loi de Beer-Lambert. Activités TP |
|
Activité expérimentale
- Une fois vos mesures terminées débrancher le câble reliant la carte à l'ordinateur. Document 3 : loi de Beer-Lambert. Lorsque la concentration est assez |
|
1 • Réaliser une gamme étalon de bleu patenté V (additif alimentaire
3. Modéliser les données expérimentales en utilisant la loi de Beer-Lambert. Dissoudre un bonbon gélifié bleu dans de l'eau distillée. Ajuster |
|
TRAVAUX PRATIQUES DE SPECTRO- COLORIMETRIE
TP n° 3. LOI DE BEER LAMBERT - FORMULATION D'UN COLORANT. A – RAPPELS THEORIQUES. Les mélanges de colorant absorbants non diffusants constituent des mélanges. |
|
TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
Cet appareil s'appelle un colorimètre (ou spectrophotomètre). Il compare l On obtient alors une loi appelée loi de Beer-Lambert : A = ε×l×c. Le ... |
|
T.P. en Première S (option sciences expérimentales) Vérification de
Aussi après réflexion |
|
TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
Cet appareil s'appelle un colorimètre (ou spectrophotomètre). On obtient alors une loi appelée loi de Beer-Lambert : A = ?×l×c. |
|
Spectrophotométrie : Loi de beer-Lambert et suivi cinétique dune
Il s'agit d'étudier expérimentalement la relation entre la concentration effective d'une espèce colorée en solution et l'absorbance de cette solution pour une |
|
Le bleu des bonbons Schtroumpfs
Extrait du programme de première S : OBSERVER / Matières colorées. Notions et contenus courbe d'étalonnage en utilisant la loi de Beer-Lambert. |
|
Vérification de la loi de Beer-Lambert
Exemple de dilution réalisable pour la première solution à concentration finale « Cf=05 x 10-3 mol/L (volume final Vf=100mL) » : • Prélever un volume Vi=2 |
|
OBSERVER : Notions compétences et activités (première S).
21 nov. 2016 Activités TP |
|
Activité expérimentale
Document 3 : loi de Beer-Lambert. Lorsque la concentration est assez faible une relation mathématique permet de relier l'absorbance et la concentration :. |
|
Première S
TP 08 Chapitre 05 : Comment déterminer le % massique de cuivre dans une pièce de 10 cents ? La loi de Beer-Lambert indique que pour une longueur. |
|
Exercices de révisions : Physique-chimie
Le diiode I?2 (aq) réagit avec les ions thiosulfate S?2?O?3?. 2-?. (aq) pour former des ions iodures I?-? d) C'est la loi de Beer-Lambert. A = k .c. |
|
1 • Réaliser une gamme étalon de bleu patenté V (additif alimentaire
3. Modéliser les données expérimentales en utilisant la loi de Beer-Lambert. Dissoudre un bonbon gélifié bleu dans de l'eau distillée. Ajuster |
|
TP en Première S (option sciences expérimentales) Vérification de
T P en Première S (option sciences expérimentales) Vérification de la loi de Beer-Lambert sans spectrophotomètre par Nicolas SOLIGNY |
|
TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
On obtient alors une loi appelée loi de Beer-Lambert : A = ?×l×c Le coefficient directeur de la droite correspond au produit ?×l |
|
TP C1 : Spectrophotométrie Loi de Beer-Lambert - Free
22 sept 2005 · Résumé Le but de ce TP est de (re)découvrir expérimentalement la loi de Beer- Lambert qui établit une relation entre absorption |
|
La loi de Beer - Lambert
Ecrire explicitement la loi de Beer-Lambert -Mesurer l'absorbance à la longueur d'onde indiquée d'une solution inconnue du sel qui vous sera distribuée et |
|
TP C1 : Spectrophotométrie Loi de Beer-Lambert - DocPlayerfr
1 TP C1 : Spectrophotométrie Loi de Beer-Lambert Gabriel Scherer TS3 22 septembre 2005 Résumé Le but de ce TP est de (re)découvrir expérimentalement la loi |
|
Activité expérimentale
Document 3 : loi de Beer-Lambert Lorsque la concentration est assez faible une relation mathématique permet de relier l'absorbance et la concentration : |
|
TP de physique-chimie Première Spécialité
6 Tracer la courbe d'étalonnage A = f(c) et vérifier si elle est conforme `a la loi de Beer-Lambert Quelle est la valeur et l'unité du coefficient de |
|
Dosage par étalonnage loi de Beer-Lambert
Dosage par étalonnage Loi de Beer-Lambert Objectifs du T P : Savoir calculer une masse à dissoudre pour obtenir une solution de concentration donnée |
|
Loi de Beer-Lambert - Eduscol
Tester les limites de linéarité de la loi de Beer-Lambert pour des solutions diluées de colorants alimentaires Page 4 Lycée voie(s) Générale Technologique |
|
TP évalué beer lambert - Travaux pratiques - Chimie Physique - 1ère
TP évalué 1ère S Dissolution échelle de teinte mesure d'absorbance loi de beer lambert Télécharger au format PDF Télécharger le fichier original |
Comment calculer avec la loi de Beer-Lambert ?
Rappeler la loi de Beer-Lambert
Parfois, la loi de Beer-Lambert est écrite sous la forme A = k \\times C dans laquelle la constante k est le produit du coefficient d'extinction molaire \\varepsilon et de la longueur l de solution traversée : k = \\varepsilon \\times l.Comment mesurer l'absorbance TP ?
On utilise comme matériel un spectrophotomètre. Le spectrophotomètre sélectionne une radiation monochromatique (une seule longueur d'onde ?) à travers une cuve de longueur l de solution et mesure l'absorbance A de la solution. Il faut régler le zéro en pla?nt le solvant (eau) dans la cuve.- La loi de Beer-lambert s'applique pour des radiations monochromatiques et sa validité est bonne losqu'on travaille avec des solutions diluées (la loi est une loi limite à "dilution infinie et interactions nulles").
|
Dosage - Lycée dAdultes
14 déc 2019 · 1ère spécialité Physique-Chimie - Lycée d'adultes - Poisson Florian 14 décembre (b) La loi de Beer-Lambert est-elle vérifiée? La courbe |
|
Absorption, absorbance, et dosage - Fiche professeur
Loi de Beer-Lambert et application au dosage de solutions colorées Type d' activité : Activité expérimentale Conditions de mise en œuvre : Séance de travaux |
|
Devoir surveillé n°2 – Octobre 2012 / 20 pts - Free
Les grandeurs physiques absorbance A et concentration molaire c sont liées par la loi de Beer-Lambert A = ε l c où ε est le coefficient d'extinction molaire et la |
|
Loi de Beer-Lambert - Prophychi - Free
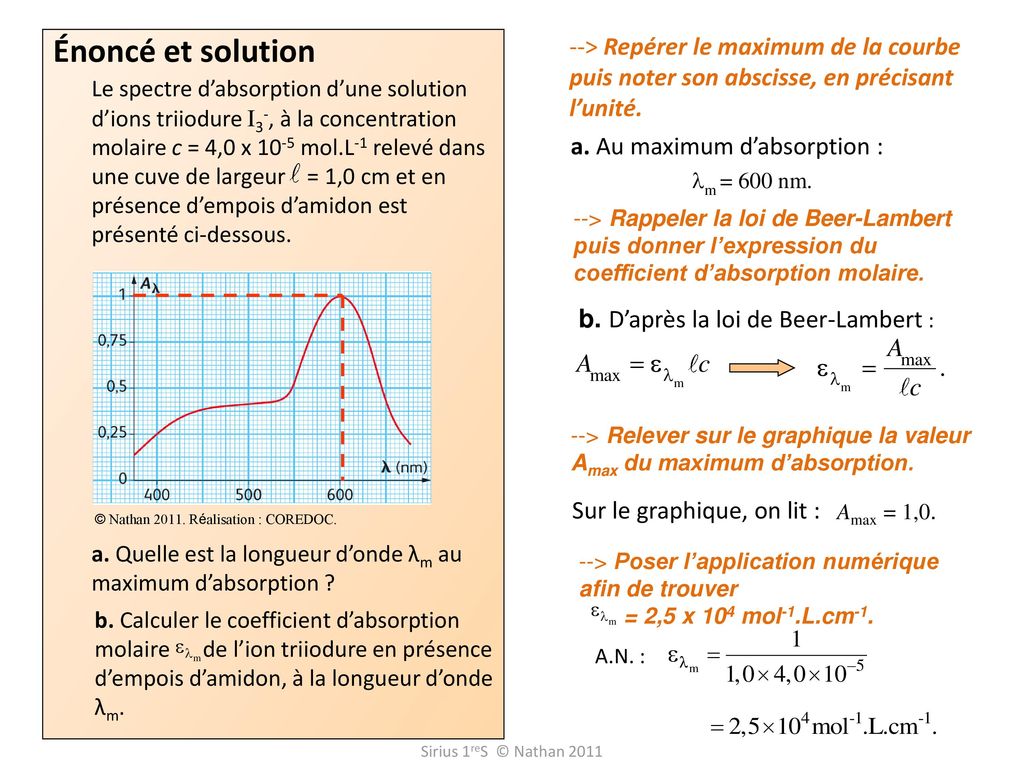
Elle se mesure avec un spectrophotomètre Première S http://prophychi free H Abbès Le spectre d'absorption d |
|
Exercices sur les matières colorées - Lycée Maurice Ravel
Donc A est proportionnelle à c, c'est la loi de Beer Lambert : A = k × c 3 Mesure de la concentration de la solution de dichromate de potassium : Par lecture |
|
Télécharger ce fichier pdf - Labolycée
La concentration en ions cuivre (II) est proportionnelle à la masse de cuivre utilisée (conservation de la matière) et aussi à l'absorbance (loi de Beer-Lambert ) |
|
EPREUVE DEXERCICES DAPPLICATION - Remedeorg
D'après la Loi de Beer Lambert : ε 1 C A = :ε coefficient d'absorption spécifique 1 : trajet optique = 1 cm C : concentration de la solution mesurée : g L-1 |