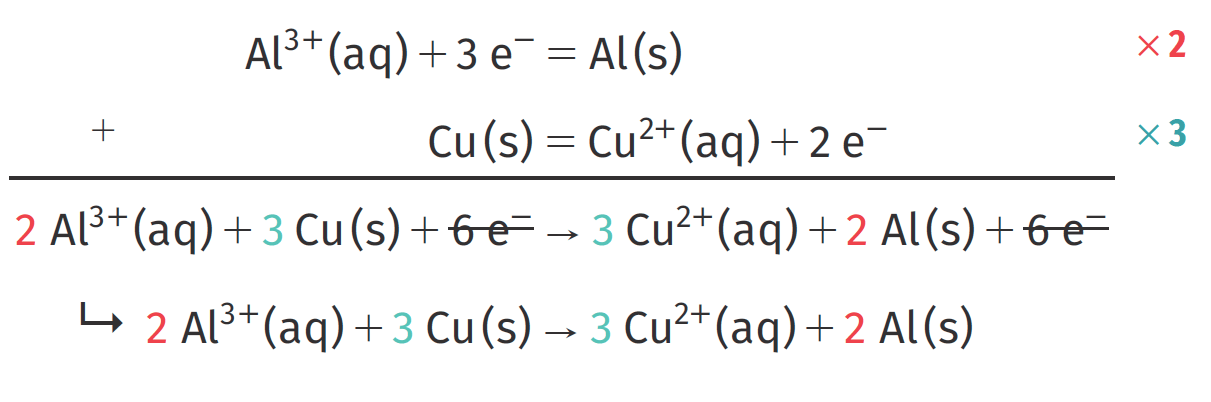exercice sur oxydoreduction/pile
|
Thème : Piles et électrolyses Fiche 4
Dans la pile les cations circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse ▻ Exercice n°2 1) Les électrons |
Comment trouver la polarité d'une pile ?
Pour trouver expérimentalement les polarités de la pile, on branche un voltmètre à ses bornes.
Si celui-ci indique une valeur négative, alors on l'a branché à l'envers.
Avec un branchement correct, la borne « com » (négative) du voltmètre est reliée à l'électrode de zinc.
La borne positive est l'électrode de cuivre.Comment équilibrer une réaction d'oxydoréduction ?
1: Écrire l'oxydant et le réducteur de part et d'autre d'une double-flèche. 2: Équilibrer les atomes autres que l'oxygène et l'hydrogène . 3: Équilibrer les atomes d'oxygène en ajoutant autant de molécules de H2O dans l'autre côté. 4: Équilibrer les atomes d'hydrogène en ajoutant autant des ions H+ de l'autre côté.
Pour fabriquer une pile électrochimique, il suffit d'immerger deux métaux différents dans des électrolytes contenant leurs propres ions Mn+ , et relier ces deux électrolytes par un pont salin.
Comment calculer une oxydoréduction ?
oxydant + ne– = réducteur
Ag+ + e– = Ag.
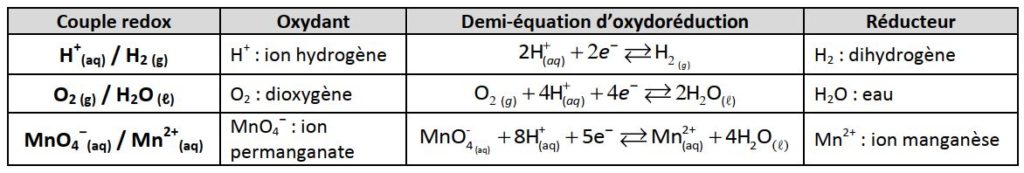
Un couple oxydant/réducteur est l'ensemble d'un oxydant et d'un réducteur conjugués, qui se transforment l'un en l'autre lors d'un échange d'électrons.
Cette transformation se réalise selon une demi-équation d'oxydoréduction.
|
Sentraîner : Piles et oxydoréduction Exercice : Laccumulateur au
S'entraîner : Piles et oxydoréduction. Exercice : L'accumulateur au plomb et le démarrage automobile. La batterie d'une voiture est un accumulateur au plomb |
|
Exercices de la séquence n°4 - Piles
EXERCICE 1 : vrai ou faux ? 1. Une réaction d'oxydoréduction a lieu lorsque la pile débite du courant. 2. À la surface de l' |
|
EXERCICES SUR OXYDOREDUCTION / PILES
EXERCICES SUR OXYDOREDUCTION / PILES. EXERCICE 1 : On dispose des produits suivants : fil d'argent lame de fer |
|
LES REACTIONS DOXYDOREDUCTION Exercice 1 (Daprès BTS
CORRECTION EXERCICES DE REVISION : LES REACTIONS D'OXYDOREDUCTION. Exercice 1 (D'après BTS ABM 2001 Etude d'une pile). 1. Schéma de la pile :. |
|
EXERCICES SUR OXYDOREDUCTION / PILES
EXERCICES SUR OXYDOREDUCTION / PILES. EXERCICE 1 : On dispose des produits suivants : fil d'argent lame de fer |
|
Exercices sur les piles et loxydore duction Exercices sur les piles et
redox mis en jeu. 2. Déterminer la quantité d'ions hydrogène H+ présents dans la solution d'acide chlorhydrique. |
|
Exercices de révision- Oxydo-réduction et Piles électrochimiques
Exercice I. On considère la pile symbolisée par: Cu / Cu2+ (01M) // Fe2+ (0 |
|
TD : Oxydoréduction et piles
Exercice 6 : Utiliser la polarité d'une pile. On considère la pile zinc-argent ci-dessous. 1. Déterminer le sens du courant la nature des porteurs de charges |
|
Piles et accumulateurs oxydoréduction
Exercice 8 p.298 1. La cathode est l'électrode po- sitive ici |
|
Piles et oxydoréduction Exercice - Lycée Ismael Dauphin
S'entraîner : Piles et oxydoréduction Exercice : L'accumulateur au plomb et le démarrage automobile La batterie d'une voiture est un accumulateur au plomb, |
|
Exercices sur les piles et loxydore duction Exercices sur les piles et
redox mis en jeu 2 Déterminer la quantité d'ions hydrogène H+ présents dans la solution d'acide chlorhydrique |
|
Oxydoréduction – corrigé des exercices Table des matières
Quelle est la masse de Zn qui disparaît pendant le fonctionnement de la pile ? Réponses : a La réaction d'oxydation est attribuée au couple qui possède E° le |
|
LES REACTIONS DOXYDOREDUCTION Exercice 1 - PC-STL
CORRECTION EXERCICES DE REVISION : LES REACTIONS D' OXYDOREDUCTION Exercice 1 (D'après BTS ABM 2001 Etude d'une pile) 1 Schéma de la |
|
Oxydoréduction Oxydoréduction - Étienne Thibierge
2 mai 2018 · le seuil limite Exercice 6 : Pile argent-zinc [♢00] On s'intéresse à la pile schématisée par Ag(s)Ag +(c)Zn2+(c )Zn(s) avec c = 0,18 mol · L−1 |
|
TD : Oxydoréduction et piles
Piles : Exercice 6 : Utiliser la polarité d'une pile On considère la pile zinc-argent ci-dessous 1 |
|
Les piles et loxydo-réduction :
On négligera la différence de potentiel de jonction et on confondra les notions d' activité et de concentration On donne les potentiels normaux des couples redox : |